氢氧化铁:一种导致绿锈的化合物
简介
铁在有水分的情况下与氧气结合就会形成铁锈。它通常与铁基物体的腐蚀有关,如屋顶、钉子和汽车。它的颜色范围很广,包括黄色、棕色、橙色和红色。
你知道有一种锈是绿色的吗?它是由氢氧化铁(含少量氧)引起的。氢氧化铁(II)是什么?继续阅读以了解更多信息。
氢氧化铁是什么?
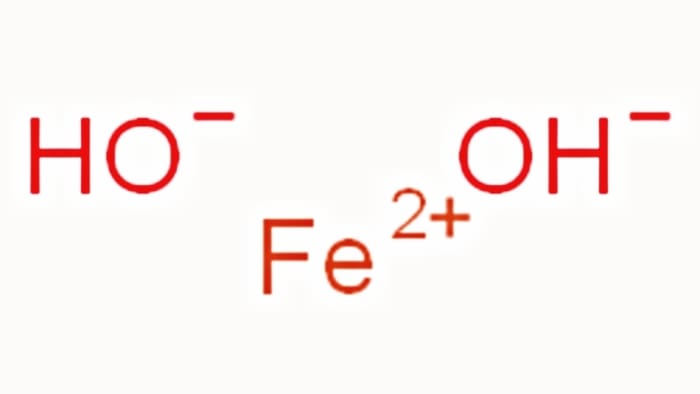
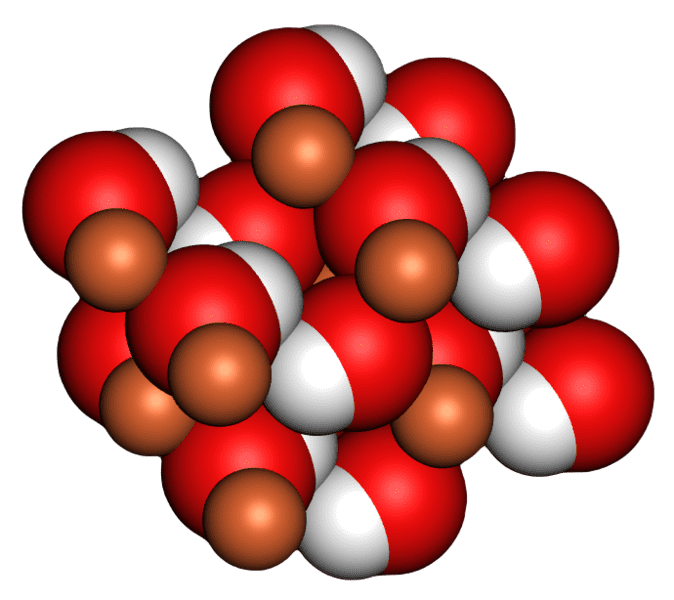
氢氧化铁(II),也称为氢氧化铁,是一种无机化合物,由一个处于第二氧化态的铁原子(铁的两个价电子与其他离子、原子或分子相连)和两个氢氧根阴离子组成。它的化学式是Fe(OH)2.纯氢氧化铁通常以白色凝胶、粉末或三角形晶体的形式存在。当它与空气中的氧气接触时,就会变成一种绿色的物质,叫做绿锈。
氢氧化铁(II)是空气中的氢氧根离子与铁或钢表面相互作用形成的。然而,由于氢氧根离子在空气中的稀缺性,氢氧化铁在人类制造的铁基物品中也不常见。尽管如此,它在潮湿的环境中丰富,有许多含铁的岩石,在那里,空气中的水、铁和氧气随着时间自发地相互作用。它也可以以各种矿物的形式被发现,如阿木质岩。
氢氧化铁(II)可以在实验室中以多种方法合成,包括通过反应铁盐,如氯化亚铁(FeCl)2),含有氢氧根离子的物质,如碱液(氢氧化钠,NaOH)。它也可以作为其他化学反应的副产品产生。稍后,我们会讲到一系列可以用来合成Fe(OH)的反应物和试剂2以及它们的化学方程式。
氢氧化铁(II)的其他性质及潜在危害
氢氧化铁(II)的密度为3.4 g/cm3.分子质量为89.86 g/mol。它有一个角或v形的分子结构。它不溶于水和许多其他溶剂。它不会在火中燃烧。当加热到150摄氏度时,它会分解成两种成分:氧化铁(Fe₂O₃;II或III)和氢。然而,它的组成部分分离还需要很长一段时间。有时,这可能需要两个小时。
这个薄弱的基础并不构成重大威胁。当大量的纯氢氧化铁与皮肤接触时,它会引起轻微的不适,如果食用,还会引起轻微的胃部问题。事实上,它被用作纹身颜料和不同浓度的口服药物。
合成铁(II)的生产
在实验室中,可以通过以下反应物和试剂合成氢氧化铁:
1.硫酸铁(II)与氢氧化钾反应可生成氢氧化铁(II)和硫酸钾。
- FeSO4+ 2 KOH→Fe (OH)2+ K2所以4
2.氯化铁与氢氧化钾反应可生成氢氧化铁(II)和氯化钾。
- FeCl2+ 2 KOH→Fe (OH)2+ 2 KCl
3.铁、水和氧反应可以产生氢氧化铁(II)。
- 2 Fe + 2 Н2О + o2→Fe (OH)2
4.硫酸铁(II)与氢氧化钠反应生成氢氧化铁(II)和硫酸钠。
- FeSO4+ 2 NaOH→Fe (OH)2+钠2所以4
硫酸铁与氢氧化钠反应生成氢氧化铁
应用程序
氢氧化铁具有改善水质、减少水污染的潜力。研究表明,氢氧化铁可以去除水体中有害有毒的亚硒酸盐和亚硒酸盐离子。当铁(哦)2与这些硒离子反应,它降解成无害的元素硒和其他无害的矿物质和物质。
除了纹身,氢氧化铁还被用作颜料、玻璃和化妆品的色素。它也可以用于医疗领域。氢氧化铁聚糖是氢氧化铁的一种口服药物形式,可用于治疗贫血和其他由缺铁引起的疾病。此外,氢氧化铁(II)在农业中可作为肥料,并可帮助缺铁的植物。它也用于镍铁电池,湿地净化,疏通下水道和管道。
资料来源及进一步阅读
- 氢氧化铁|科学直接课题概述
这篇文章涵盖了与氢氧化铁和其他相关矿物有关的广泛主题。它涵盖了它们的特征、制造、来源和化学成分,以及采矿和化学反应造成的环境破坏。 - 氢氧化铁:特征,性质,生产和化学反应|科学Alpha
本文讨论了Fe(OH)2的特性、性质、生产方法及化学反应。 - 从水溶液中选择性去除硒离子的方法——谷歌专利
本文描述了从含有硒离子的水溶液中选择性消除硒离子的方法,涉及与一定量的亚铁离子接触,使硒离子还原为元素硒。
- 铁(II)氢氧化铁聚麦芽糖|
片剂Wise提供有关铁(II)氢氧化铁聚麦芽糖的信息,氢氧化铁的口服药物形式。 - 氢氧化铁(Fe(HO)2) |的性质
本文介绍了氢氧化铁的结构、物理和化学性质、生物活性、安全和危害信息等 - 绿锈:它是什么,它是如何工作的| Thoughtco
这个Thoughtco页面提供了关于锈病的信息,尤其是绿色锈病。
- 氢氧化铁| Prezi
这个Prezi页面有一个幻灯片,上面有很多关于Fe(OH)2的信息,你可以在幻灯片演示中使用。
据作者所知,这些内容是准确和真实的,并不意味着要取代来自合格专业人士的正式和个性化的建议。
©2022 Errah Caunca